實時活細胞成像的好處
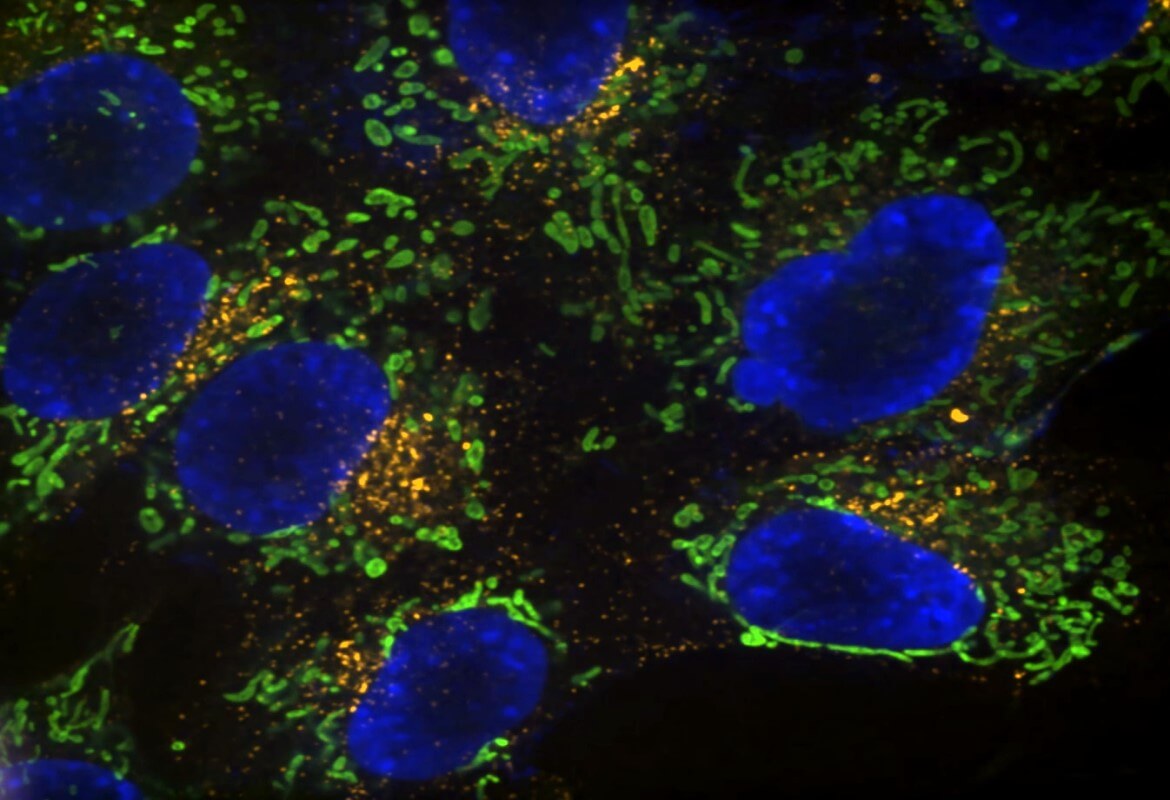
基於三維 (3D) 細胞的分析取代了許多組織、細胞和動物測試模型,但因缺乏時間分辨率而聞名。例如,傳統的基於細胞的終點實驗將測試化合物的劑量與方便(有時是任意)時間點的暴露相關聯,這無法解決動力學的相關性。因此,實時活細胞分析可以捕捉發生的生物變化,從而為回答因果關係的關鍵問題提供更多信息。
解卷積細胞死亡
評估細胞毒性潛力是一種在藥物發現過程中評估化合物的長期方法。了解細胞毒性及其相關機制對於調節穩態過程(例如耐受性和免疫原性細胞死亡)或當細胞死亡過程與疾病有關時非常重要。由於細胞死亡是通過一系列不同的生物學線索開始的,最終導致膜完整性的喪失,因此識別該過程中涉及的生物標誌物變得至關重要。
細胞凋亡是一種耐受性的細胞死亡形式,在化療誘導的癌細胞死亡中是理想的。磷脂酰絲氨酸 (PS) 是一種可用於表徵凋亡表型的生物標誌物,因為它僅存在於健康細胞的內膜小葉內,但在細胞凋亡早期易位至外膜。在這個階段,膜的完整性將重要的染料拒之門外。隨著細胞死亡隨著時間的推移而進行,細胞會失去膜的完整性,表明它們已經死亡。發光和熒光信號的這種時間分離有助於確定凋亡或其他機制是否在起作用。
經常通過基於細胞計數的方法研究細胞凋亡,使用對 PS 具有固有親和力的膜聯蛋白 V 探針或用於量化死細胞的核染色。這些方法很有用,但需要費力的染色、洗滌、分析和數據分析,這限制了通量。基於實時細胞的檢測,如 Promega 的基於微量滴定板的 RealTime-Glo™ Annexin V Apoptosis and Necrosis Assay,允許對 PS 和核染色進行近乎連續的監測,以建立細胞死亡機制、反應幅度和動力學,而無需取樣或銷毀測試單元。
該測定使用發光來測量 PS 暴露,並使用熒光來量化膜完整性的損失。通過在適當配置的儀器上應用明場和熒光成像可以進一步增強這些強度值。成像可以通過闡明與特定形式的細胞死亡相關的形態特徵來補充板強度測量。
“實時、非破壞性方法允許您在整個細胞暴露過程中從同一測定孔重複收集數據。因此,單板實驗可以提供數千個數據點,並提供必要的分辨率來充分錶徵凋亡反應,”Promega 研究科學家 Drew Niles 說。“其他傳統方法需要多個檢測板、更大的消耗品流和相當大的操作員工作量。”
RealTime-Glo 檢測基於二元熒光素酶系統的互補,基因表達為不同的膜聯蛋白 V-NanoBiT 融合體。啟用試劑是 NanoLuc 螢光素酶,這是一種源自蝦的新型生物發光酶,比螢光素酶更小更亮。其明亮的信號和微小的尺寸 (19kDa) 使研究人員能夠可視化少量蛋白質,同時對細胞和分子功能的破壞最小。
在一個例子中,卡爾加里大學的 Li-Fang Chu 教授使用 NanoLuc 在 24 小時內錄製相同活細胞的視頻,以實時可視化參與人類發育分割的靶基因表達的上升。另一項研究強調了流感病毒在小鼠肺部增殖的實時動力學。根據 Niles 的說法,NanoLuc 螢光素酶幫助這些研究人員克服了報告病毒的不穩定性和有限的敏感性。
方法的匯合
缺乏與生理相關的人腦模型阻礙了治療常見神經系統疾病的藥物的開發。由於乾細胞和三維 (3D) 細胞培養,這種情況應該會有所改善。誘導多能幹細胞 (iPSC) 分化方案現在允許創建幾乎所有人類腦細胞亞型,而類器官等 3D 培養物的優化提供了一個適合基礎研究的平台,包括藥物篩選。
總之,這些發展導致了類器官模型的發展,這些模型模仿了新生兒大腦的顯著特徵,作為大腦發育和神經系統疾病的模型。
實驗模型雖然必不可少,但通常過於復雜,甚至不適用於中等通量藥物或毒理學篩選,更不用說高通量篩選 (HTS) 藥物開發人員的需求了。Molecular Devices的 應用說明描述了一種適用於多種化合物 HTS 的神經毒性測定。重要的是,該模型在每個數據點使用少量單元格。
“這種平台的關鍵先決條件包括與自動化高內涵成像設備的兼容性和相對快速的讀數,”Molecular Devices 的高級科學家 Oksana Sirenko 博士解釋說。“此外,該模型應在每個數據點利用有限數量的細胞材料,同時仍將人腦的複雜性模擬到獲得生理相關反應所需的程度。”
該說明描述了一種新型微流體微量滴定平台,使用MIMETAS OrganoPlate® ,該平台 由在 384 孔微孔板中培養的 96 個 3D 神經元神經膠質網絡組成。每個包含神經元細胞、神經膠質細胞和細胞外基質 (ECM) 共培養物的孔都與其他四個孔相連:一個提供細胞/ECM 混合物,兩個提供生長培養基,而第四個保留用於免疫熒光成像。
在 OrganoPlate 中,3D 神經元膠質類器官很容易形成範圍廣泛的終末分化神經元幹細胞,適用於測定自發神經放電,以及評估添加的化合物對電生理學、細胞活力和神經突生長的影響。
“有幾種用於神經元細胞研究的常見模型,包括原代神經細胞和 iPSC 衍生的神經細胞,以及類似於大腦結構和組織的 3D 神經球體或 3D 大腦類器官微組織,”Sirenko 說。
由於神經突網絡的複雜性,對二維培養中的神經元細胞進行成像和分析已經非常具有挑戰性。應用高內涵成像和神經突生長分析算法可以計算培養中神經元的密度,以及神經網絡的複雜性、分支和過程的數量,以及細胞體的數量和神經元細胞的活力。
3D 細胞培養對神經元培養的成像和分析提出了更大的挑戰。神經網絡可以在 3D 矩陣中生長,然後進行共焦成像和圖像分析以評估這些網絡。
源自 iPSC 的神經元可以形成長到 4 毫米大小的大腦類器官,這進一步增加了複雜性。“光對厚樣品的穿透力是有限的,而且圖像被不同視野中細胞的光散射所淹沒,”Sirenko 補充道。“通常,共焦成像用於最大限度地減少來自不同焦平面的光散射,而具有水浸功能的強大激光光學元件能夠產生更強的信號、更大的光穿透性和更高的圖像質量。”
最有趣(儘管具有挑戰性)的研究涉及使用鈣成像測量神經元的功能活動。激活後,鈣進入和離開細胞間室,可以通過鈣敏感染料或內部表達的鈣傳感器觀察到。
“通過延時成像可以觀察到神經活動的峰值,”Sirenko 告訴 Biocompare,“並且可以通過它們的峰值強度、頻率和幅度進行視覺記錄和分析。尖峰可能不同步和稀疏,或者是同步的並且可能涉及整個微組織。鈣流的強度和模式可以通過各種神經活性或神經毒性化合物進行調節;因此,該檢測方法可能對測試神經性藥物或毒素具有重要價值。”
根據 Sirenko 博士的說法,這種方法的一個額外的(有些人可能會說很關鍵)的好處是能夠執行時間進程記錄,這可以在幾分之一秒的時間間隔內完成。“生物學的當前趨勢是增加分析模型的複雜性,以更好地概括組織和器官的複雜性,並更好地了解生物學。因此,儀器需要增加容量和復雜性,以使科學家能夠從他們的分析中獲得最大量的有用信息。”